
Edelmetalle spielen in der chemischen Industrie eine wichtige Rolle als Katalysatoren: Mit Hilfe von Silber, Platin, Palladium oder anderen Elementen kann man chemische Reaktionen ablaufen lassen, die sonst nicht oder nur mit viel geringerer Reaktionsrate voranschreiten würden. Oft setzt man diese Metalle in Form winziger Nanopartikel ein. Wie gut sie wirken, hängt allerdings auch vom Untergrund ab, auf dem sie platziert werden. Nanopartikel auf einer Kohlenstoff-Unterlage scheinen besonders gut zu funktionieren - der Grund dafür war lange Zeit unbekannt.

Von ,,schwarzer Kunst" zur Wissenschaft
,,Der Einsatz von Kohlenstoff als Trägermaterial für die Katalyse hatte lange Zeit fast etwas Magisches", sagt Günther Rupprechter vom Institut für Materialchemie der TU Wien. Die Herkunft des Kohlenstoffs stellte sich als wichtig heraus: Für manche Prozesse setzte man etwa Kohlenstoff ein, der aus Kokosnuss-Schalen, -Fasern oder speziellen Hölzern gewonnen wurde. Sogar in offiziellen Patentschriften sind solche ,,Rezepturen" zu finden - dabei sollte die Herkunft chemischer Substanzen doch eigentlich relativ egal sein. ,,Es erschien immer ein bisschen wie schwarze Kunst", sagt Günther Rupprechter.Die Idee dahinter war, dass unterschiedliche Herstellungsmethoden zu minimalen chemischen oder physikalischen Unterschieden führen könnten: Vielleicht ordnet sich der Kohlenstoff je nach Herstellungsart auf unterschiedliche Weise an’ Vielleicht enthält er Spuren anderer chemischer Elemente’ Oder an der Oberfläche lagern sich funktionale Gruppen an - kleine molekulare Bausteine, die in die chemische Reaktion eingreifen’ ,,In der chemischen Industrie gibt man sich naturgemäß oft damit zufrieden, dass ein Prozess funktioniert und man ihn zuverlässig wiederholen kann", sagt Rupprechter. ,,Wir wollten der Sache aber auf den Grund gehen und auf atomarer Ebene genau verstehen, was hier eigentlich vor sich geht." Neben Rupprechters Team war auch das das Zentrum für Elektronenmikroskopie der TU Wien (USTEM) und die Universität Cádiz (Spanien) beteiligt.
Präzisionsmessungen in einem Mikroreaktor
Das Team stellte zunächst extrem präzise charakterisierbare Proben her: Silber-Nanopartikel bekannter Größe auf einem Kohlenstoff-Untergrund und eine dünne Silberfolie ohne Kohlenstoff.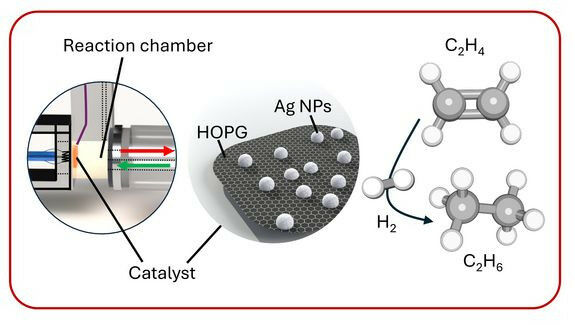
Somit konnte nun erstmals der Aktivitäts-Unterschied zwischen Silberatomen mit und ohne Kohlenstoff-Träger genau quantifiziert werden - mit spektakulärem Ergebnis: ,,Pro Silberatom erreicht man durch den Kohlenstoff-Untergrund eine zweihundertfach höhere Aktivität", sagt Thomas Wicht. ,,Das ist natürlich für industrielle Anwendungen sehr wichtig. Man braucht nur ein Zweihundertstel der Menge an teuren Edelmetallen, um dieselbe Wirkung zu erzielen - und das einfach, indem man vergleichsweise kostengünstigen Kohlenstoff dazu nimmt."
Der spannende Effekt passiert genau an der Grenze
Alexander Genest aus dem TU Team führte entsprechende Computersimulationen durch, die die Aktivierung von Wasserstoff durch Silber Nanopartikel auf Kohlenstoff und reinem Silber vergleichen. Dadurch wurde klar: Entscheidend ist die Grenzregion zwischen Silberpartikel und Kohlenstoff-Träger. Genau dort, wo beide in Kontakt treten, ist die Katalysator-Wirkung am größten. ,,Es liegt also nicht an der Größe der Kohlenstoff-Oberfläche oder an irgendwelchen Fremdatomen oder funktionalen Gruppen. Eine extreme katalytische Wirkung tritt dann auf, wenn ein Molekül direkt an der Kontaktstelle sowohl mit einem Kohlenstoffals auch mit einem Silberatom in Berührung kommt", sagt Alexander Genest. Je größer dieser Bereich des direkten Kontakts, umso größer auch die Aktivität.
Originalpublikation
Thomas Wicht, Alexander Genest, Lidia E. Chinchilla, Thomas Haunold, Andreas Steiger-Thirsfeld, Michael Stöger-Pollach, José J. Calvino, Günther Rupprechter: The role of interfacial hydrogen in ethylene hydrogenation on graphite supported Ag, Au, and Cu catalysts; ACS Catalysis, 14 (2024) 16905-16919 https://doi.org/10.1021/acscatal.4c05246Die Arbeiten wurden vom Wissenschaftsfonds FWF gefördert [10.55776/I4434-N and 10.55776/Coe5] (Single Atom Catalysis and Cluster of Excellence Materials for Energy Conversion and Storage, MECS).





